Brown Arreola, Berenice
Rodriguez Medina, Julia
Pérez García, Esther
DEFINICIÓN
El espacio pleural es una cavidad virtual situada entre el pulmón y la pared torácica, donde en condiciones normales existe un volumen de 10-15 ml de líquido pleural por cada hemitórax, disponiéndose entre las dos superficies pleurales y permitiendo el deslizamiento de una sobre otra con los movimientos respiratorios. Se entiende por derrame pleural al acúmulo patológico de líquido en la cavidad pleural. El derrame pleural no es una enfermedad en sí misma, sino la expresión de múltiples enfermedades.
ETIOPATOGENIA
El líquido de las capas pleurales está determinado por la presión hidrostática y osmótica de los capilares, drenaje linfático y el estado de las membranas basales. Cuando hay una alteración en este balance, se produce un cúmulo de líquido dando lugar al aparecimiento del DP.
Diferentes situaciones patológicas son las que pueden conducir a la acumulación de líquido por diferentes mecanismos etiológicos:
- Aumento de la presión hidrostática de los capilares de la circulación pulmonar, como ocurre en la insuficiencia cardiaca con fallo del ventrículo izquierdo, dando lugar a trasudados.
- Disminución de la presión oncótica de la sangre, sobre todo por hipoalbuminemia, dando lugar a trasudados.
- Paso de líquido desde cavidad peritoneal, dando lugar a trasudados.
- Dificultad y/o obstrucción del drenaje linfático (fallo del ventrículo derecho, SVC, linfangitis carcinomatosa).
- Aumento de la permeabilidad capilar a nivel pleural, por patología de la propia pleura (infecciosa, neoplásica, etc. ), dando lugar a exudados predominantemente.
- Rotura anatómica con vertido de líquido a la cavidad pleural (hemotórax, quilotórax, derrames yatrogénicos).
| MECANISMO | EJEMPLO |
| Aumento de presión hidrostática sistémica | Insuficiencia cardiaca |
| Disminución de la presión oncótica | Hipoalbuminemia, Sd. Nefrótico |
| Aumento de la permeabilidad capilar en la circulación pleural | Tuberculosis, metastasis pleurales |
| Obstrucción drenaje linfático | Masas mediastínicas |
| Paso de líquido desde otras cavidades | Hidrotorax hepático |
| Aumento presión negativa espacio pleural | Pulmón atrapado |
| Rotura/compresión conducto torácico | Quilotórax |
| Rotura vascular | Hemotórax |
DIAGNÓSTICO DEL DERRAME PLEURAL
| HISTORIA CLÍNICA | SÍNTOMAS | EXPLORACIÓN FÍSICA |
| – Hábitos tóxicos.
– Exposición laboral. – Uso de medicamentos. – Patologías previas. – Semiología infecciosa. – Enfocado por aparatos y sistemas. |
– Disnea.
– Tos no productiva. – Dolor torácico de tipo pleurítico. – Puede cursar asintomático. |
TRIADA PLEURÍTICA.
– Disminución del MV. – Disminución o abolición de vibraciones vocales. – Matidez a la percusión.
|
PRUEBAS COMPLEMENTARIAS
Los métodos de imagen aportan información sobre el tamaño, extensión y naturaleza del derrame pleural.
| RX DE TÓRAX PA Y LATERAL | ECOGRAFÍA TORÁCICA | TC DE TÓRAX |
| – Técnica de valoración inicial.
Puede ser visible a partir de 75-100ml.
Hallazgos: – Forma de menisco con concavidad cóncava. – Borramiento seno costofrénico ipsilateral. – DP masivo: Pulmón blanco con desplazamiento mediastínico contralateral. |
– Puede ser realizada a pie de cama.
– Permite diagnóstico diferencial entre DP, atelectasia o elevación diafragmática. – Determinar características del líquido pleural sugestivo de exudado. (Derrames loculados, encapsulados o con septos). – Estimar el volumen del derrame (detectándolo a partir de 5ml aprox.) – Localizar el punto de punción para su estudio. |
– Se recomienda su realización con contraste intravenoso.
– Permite la caracterización pleural más detallada, así como mostrar la existencia de lesiones pulmonares subyacentes. – Localización detallada de la cámara de derrame pleural en caso de necesidad de DET. |
DIAGNÓSTICO ETIOLÓGICO
Toracocentesis diagnóstica:
Procedimiento diagnóstico inicial en todo derrame pleural excepto en casos en los que sean bilaterales con alta sospecha de trasudado (ICC, sd. nefrótico, hepatopatía, diálisis peritoneal) donde se llevará a cabo sólo en caso de dudas diagnósticas o evolución desfavorable a pesar de tratamiento dirigido intensificado.
- Contraindicaciones relativas: INR >1.5, Trombocitopenia < 50.000
- Complicaciones más frecuentes: reacción vagal (10-14%) , neumotórax (3-8%).
Valorar aspecto macroscópico.
| AMARILLENTO O SEROFIBRINOSO | SUGIERE EXUDADO O TRASUDADO |
| Purulento, verdoso o maloliente | Empiema. |
| Sero hemorrágico que no coagula espontáneamente | Neoplásico o paraneumónico. |
| Sero hemorrágico que coagula espontáneamente | Hemotórax. |
| Líquido aspecto lechoso | Quilotórax o seudoquilotórax. |
Se recomienda que sea ecoguiada, puncionando por el borde superior de la costilla inferior y se debe enviar 3 muestras independientes a:
- Bioquímica: Glucosa, LDH, ADA, proteínas e incluir jeringa de gasometría para pH.
- En caso de sospecha de:
- ICC: añadir proBNP.
- Quilotórax: solicitar colesterol, triglicéridos y quilomicrones.
- Microbiología: Tinción gram, microscopía y cultivo.
- Citología: Realizar petición de anatomía patológica.
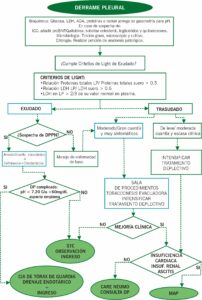
Criterios de Light:
Permite realizar el diagnóstico diferencial entre exudado y trasudado.
- Relación proteínas totales LP/ proteínas totales suero > 0.5.
- Relación LDH LP / LDH suero > 0.6.
- LDH en LP > ⅔ de su valor normal en plasma.
| EXUDADO | TRASUDADO |
| Si cumple alguno de los criterios de Light (Sensibilidad cercana al 100%).
Su etiología es muy variada, con mayor frecuencia de causa neoplásica, paraneumónica o infección tuberculosa. Menos frecuente: quilotórax, origen cardiovascular, enf. sistémicas, asbestosis, enf. gastrointestinales o fármacos. |
Si no cumple criterios de Light.
Las causas más frecuentes son ICC, hidrotórax hepático. Menos frecuentes: Sd. nefrótico, urinotórax, diálisis peritoneal o pulmón atrapado.. |
| PARÁMETROS | VALOR | ORIENTACIÓN DIAGNÓSTICA |
| Proteínas | Proteínas LP/ Proteínas plasma > 0.5 | Cualquier condición que cause exudado. |
| LDH | LDH LP/ LDH plasma > 0.6 | Cualquier condición que cause exudado. |
| Glucosa | < 60 mg/dl | Derrame paraneumónico complicado, empiema, neoplasia, TBC, AR, LES, Rotura esofágica. |
| pH | < 7.20 | Derrame paraneumónico complicado, empiema, neoplasia, TBC, AR, acidosis sistémica, hemotórax |
| ADA | >40 U/l | TBC, empiema, linfoma, AR |
| Amilasa | < nivel normal en suero | Neoplasia, rotura esofágica, enfermedad pancreática |
| NT- proBNP | >1500 pg/ml en LP | Insuficiencia cardiaca. |
Citología: número total de células: recuento y fórmula (un tubo). Búsqueda de células neoplásicas (tres tubos). Tabla 2.
| PARÁMETROS | VALOR | ORIENTACIÓN DIAGNÓSTICA |
| Hematíes | HTO LP/ HTO sangre >0.5 | Hemotórax |
| Linfocitos | >50% | Neoplasias, TBC, TEP, By-pass de art.coronarias |
| PMN | >50% | Paraneumónico. Fase precoz de TBC, TEP. |
| Células malignas | Presencia | Neoplasia |
| Células mesoteliales | > 5% | Descarta posible TBC |
Microbiología: en condiciones de anaerobiosis para poder realizar determinaciones de gérmenes anaerobios, aerobios, micobacterias y hongos. Se deben solicitar igualmente tinciones de Gram y de Ziehl.
TRATAMIENTO DEL DERRAME PLEURAL
TRASUDADO
Las causas potenciales de un trasudado son numerosas, aunque por lo general es la manifestación de otra enfermedad y el manejo principal debe ser el de la patología de base (ICC, sd. nefrótico, hepatopatía, diálisis peritoneal). EXCEPTO que se trate de derrame pleural masivo con compromiso de la dinámica respiratoria, ante la duda diagnóstica de patología infecciosa concomitante o persistencia de DP a pesar de tratamiento depletivo optimizado.
EXUDADO
| NO COMPLICADO | COMPLICADO | CASOS ESPECIALES |
| Cuando no presente criterios de complicación: Tratar enfermedad de base.
Si sospecha de DP paraneumónico: Iniciar antibioterapia con amoxicilina 875/ ac. clavulánico 125mg VO c/ 8 horas 5 días ó Ceftriaxona 1g/24 h +/- Azitromicina 500 mg/24 h en caso de criterios de ingreso. |
Empiema, pH <7.2, consumo de glucosa < 40mg/dL o aislamiento microbiológico.
Contactar con cirugía torácica para valoración de drenaje endotorácico. |
Insuficiencia respiratoria: Valorar toracocentesis evacuadora sin evacuar más de 1200-1500cc por riesgo de edema ex vacuo.
Contactar con cirugía torácica para valorar DET si: – Hemotórax – Quilotórax |
BIBLIOGRÁFIA
- Cabeza Serrano, A., Lobato de la Sierra, P., Rivera Gómez, S., & García Jiménez, J. D. (2022). Manual de diagnóstico y terapéutica en neumología. (4ta edición). 275-293.
- Botana Rial., M., Pérez Pallarés., J., Cases Viedma., E., López González., F. J., Porcel., J. M., Rodriguez., M., Romero Romero., B., Valdéz Cuadrado, L., Villena Garrido, V., & Cordovilla Pérez, R. (2022). Consenso de expertos SEPAR: Diagnóstico y tratamiento del derrame pleural. (Respira-Fundación Española Del Pulmón SEPAR.). 12-15.
- Chapman, S., Robinson, Grace., Stradling, J., West, S., Wrightson, J. Manual Oxford de medicina respiratoria. (3ra edición) 49- 52, 343- 345.
- Villena Garrido, V., Cases Viedma, E., Fernández Villar, A., de Pablo Gafas, A., Pérez Rodríguez, E., Porcel Pérez, J. M., … & Valdes Cuadrado, L. (2014). Normativa sobre el diagnóstico y tratamiento del derrame pleural. Actualización. Archivos de Bronconeumología, 50(6), 235-249.
- Ferreiro, L., San José, M. E., & Valdes, L. (2015). Management of parapneumonic pleural effusion in adults. Archivos de Bronconeumología (English Edition), 51(12), 637-646.
- Villena, V. G., Cases, E. V., Fernández, A. V., Pérez, E. R., Porcel, J. P., Rodríguez, F. P., … & Valdés, L. C. (2014). Recommendations of diagnosis and treatment of pleural effusion. Update. Archivos de bronconeumologia, 50(6), 235-249.