Obando Santaella, Ignacio
Valenzuela López, Constanza Camila
Fernández Hurtado, Miguel Ángel
CONCEPTO, ETIOLOGÍA, CLÍNICA Y DIAGNÓSTICO DE LA NEUMONÍA ADQUIRIDA DE LA COMUNIDAD
| NEUMONÍA ADQUIRIDA COMUNIDAD (NAC) | NAC COMPLICADA (DERRAME PLEURAL PARANEUMONICO (DPP)/NEUMONÍA NECROSANTE (NN) | |
| Concepto | Infección parénquima pulmonar en pacientes no hospitalizados en los 14 días previos o durante las primeras 48 horas de hospitalización | DPP: exudado patológico en el espacio pleural con neumonía subyacente. Complicado si invasión espacio pleural por microrganismos
NN: Aparición de focos de necrosis en áreas de consolidación |
| Etiología | – Virus respiratorios: más frecuentes en < 2 a. Pueden causar coinfecciones con bacterias. Influenza y adenovirus pueden ocasionalmente causar DPP
– Neumococo: Principal agente bacteriano en NAC típica, DPP y NN en pacientes previamente sanos. De forma más ocasional Streptococcus pyogenes (puede asociarse a síndrome de shock tóxico) y Staphylococcus aureus – Mycobacterium tuberculosis: NAC y DPP (factores epidemiológicos de riesgo, imágenes atelectásicas/adenopatía hiliares o DPP importantes con citobioquímica compatible y sin grandes elevaciones de RFA) – Mycoplasma pneumoniae y Chlamydophila pneumoniae causa frecuente de neumonías atípicas en niños de edad escolar. Ocasionalmente DPP pequeños – Colonizadores nasofaringeos (NF) de baja virulencia (Haemophilus influenzae no tipificable, estreptococos α-hemolíticos) en pacientes con bronconeumopatía crónica, cardiopatia congénita y/o neurológica con disfagia orofaríngea. En este último caso en coinfección con anaerobios – Patógenos oportunistas en los niños con mayor grado de inmunosupresión (Legionella pneumophila, Pneumocystis jirovecii, CMV, adenovirus, fúngicas…) |
|
| Clínica | – Depende de la edad ( > inespecífica en niños de menor edad) y etiología
– Signos y síntomas más habituales: fiebre de comienzo agudo, taquipnea, disnea o dificultad respiratoria, tos (suele estar ausente al comienzo del cuadro en las neumonías alveolares) y/o dolor torácico (niños mayores y DPP). La taquipnea es el signo más sensible y específico y se correlaciona con la gravedad de la neumonía. – La sintomatología abdominal (dolor, vómitos o diarrea) y cefaleas pueden ser prominentes inicialmente |
|
| Diagnóstico | – En urgencias: diagnóstico de neumonía, determinar patrón (https://guiaprioam.com/indice/neumonia-adquirida-en-la-comunidad-nac-en-pacientes-pediatricos-2017/) y si hay criterios de ingreso.
– Exploración completa, incluyendo FR, FC y SO2 – Recomendable la confirmación radiológica, aunque no es imprescindible en una primera neumonía en niños sin factores de riesgo o criterios de gravedad que puedan ser manejados y controlados en atención primaria. |
|
Tabla 1. Concepto, etiología, clínica y diagnóstico de la neumonía adquirida de la comunidad
ALGORITMO DE MANEJO EN URGENCIAS
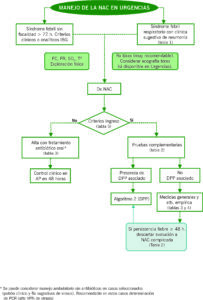
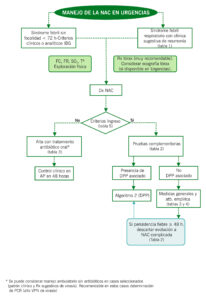
La tabla 2 y figuras 1 y 2 muestran respectivamente las pruebas complementarias recomendadas en los pacientes con criterios de ingreso y el algoritmo de manejo de la NAc y NAC complicada con DPP.
Las pruebas complementarias (análisis y microbiología) no son necesarias en la práctica clínica habitual si no hay criterios de ingreso.
| PRUEBAS COMPLEMENTARIAS EN LA NAC | |
| Analítica | – Hemograma, bioquímica, gasometría venosa (arterial/capilar si hipoxemia), reactantes de fase aguda (PCR, valorar PCT si sepsis o ingreso en UCI)
– Citobioquímia de líquido pleural (LP) (si toracocentesis) con pH (jeringa de gasometría a laboratorio) y LDH. Cursar ADA si sospecha TBC. Interpretación: https://www.aeped.es/sites/default/files/documentos/2_5.pdf |
| Imagen | – Rx tórax: AP en > 4 años y PA en > 4 años. Lateral si dudas diagnósticas o posibilidad adenopatías. Al ingreso (puede ser normal en primeras 48 horas). Si no queda afebril repetir a las 48-72 h. Patrón radiológico, extensión y despistaje de formas complicadas
– Ecografía tórax: Si derrame pleural significativo (extensión y presencia de septos). Tendencia reciente a incorporarla como prueba de primera línea para diagnóstico inicial y seguimiento evolutivo de neumonía – Tac tórax con contraste: si complicación grave, mala evolución clínica y sospecha de malformación |
| Microbiología | – Hemocultivo (previo antibioterapia) y cultivo LP (si toracocentesis). Cultivo de esputo (> 10 a.) (buena calidad:> 25 leucos/campo y 10 cél. epiteliales/campo)
– Detección antígenos en (i) orina: neumococos (considerar en > 5 a. como predictor negativo de infección neumocócica. No en< 5 a. (Falsos +). Legionellosis serogrupo 1 (pacientes inmunosuprimidos o consideraciones epidemiológicas); (ii) LP: solicitar en empiema pleural para despistaje de infección neumocócica; y iii) frotis NF/aspirado nasal en neumonías virales: VRS e influenza (preferible PCR, si disponible, por mayor sensibilidad) – Técnicas moleculares (PCR): frotis nasofaríngeo/aspirado nasal. Considerar en neumonías virales (film array), posibilidad de coinfección o de infección por M. pneumoniae si: clínica grave o criterios epidemiológicos |
| Inmunológicas | – Serología neumonías atípicas: utilidad muy limitada (no impacto sobre el manejo clínico del paciente y falsos + IgM frente a M. pneumoniae)
– Mantoux/IGRA: si posibilidad clínica/epidemiológica de TBC |
Tabla 2. Pruebas complementarias en la NAC
Figura 1. Algoritmo de manejo de la NAC en urgencias
Figura 2. Algoritmo de manejo de la NAC complicada con DPP
TRATAMIENTO DE LA NAC
Medidas generales https://guiaprioam.com/indice/neumonia-adquirida-en-la-comunidad-nac-en-pacientes-pediatricos-2017
Tabla 3. Antibioticoterapia empírica y tratamiento antiviral dirigido en la NAC
1 En NN/abscesos pulmonares duración total 4 semanas o al menos 2 semanas tras quedar afebril.
2 Si la tasa de S. aureus comunitario resistente a meticilina se incrementa a > 10% utilizar vancomicina o clindamicina y no cloxacilina.
3 Puede sustituirse por ceftriaxona IV 100 mg/kg/día cada 12-24 h (máx 4g/día).
4 En NN y síndrome de shock tóxico
CRITERIOS DE INGRESO Y DERIVACIÓN A CONSULTAS
| Criterios Ingreso Hospitalario | |
| i) Enfermedad grave: cianosis, taquipnea moderada-grave (FR > 70 rpm en < 1 año y > 50 rpm en > 1 año), dificultad respiratoria, apneas, SO2 < 92%;
ii) Patología de base: cardiopatías congénitas, enfermedad neuromuscular, respiratorias…; iii) Complicaciones pulmonares o afectación multifocal de la NAC; iv) Pérdida de tolerancia oral; v) Problema social o incumplimiento terapéutico; vi) Mala respuesta al tratamiento antibiótico tras 48 horas desde su inicio; vii) Edad < 3 meses y edad 3-6 meses con sospecha de neumonía de etiología bacteriana; viii) Individualizar en caso de etiología viral |
|
| Criterios ingreso UCI | |
| i) Inestabilidad hemodinámica;
ii) SO2 ≤ 92% a pesar de oxigenoterapia con FiO2 ≥ 0,5; iii) Apneas frecuentes o respiración irregular; iv) Hipercapnia progresiva (pCO2 ≥ 65-70, capilar o venosa); v) Afectación del nivel de conciencia |
|
| Criterios derivación a consultas | |
| i) Infectología pediátrica: neumonías graves o complicadas. Control clínico y radiológico a los 15 días y seguimiento hasta la resolución clínica y radiológica del proceso;
ii) Neumología pediátrica: neumonías recurrentes confirmadas radiológicamente |
BIBLIOGRAFÍA
- Andrés-Martín A, Escribano Montaner A, Figuerola Mulet J, et al. Documento de consenso sobre la neumonía adquirida en la comunidad en los niños. SENP-SEPAR-SEIP. Arch Bronconeumol. 2020;56:725–41.
- Montero Valladares C, Obando Santaella I, Falcón Neyra L, et al. Neumonia adquirida en la comunidad (NAC) en pacientes pediátricos; 2017 Guiaprioam.com. [citado el 2 de febrero de 2021]. Disponible en: https://guiaprioam.com/indice/neumonia-adquirida-en-la-comunidad-nac-en-pacientes-pediatricos-2017/
- Moreno-Pérez D, Andrés Martín A, Tagarro García A, Escribano Montaner A, et al. Neumonía adquirida en la comunidad: tratamiento ambulatorio y prevención. An Pediatr. 2015;83:439.e1-
- Moreno Pérez D, Andrés Martín A, Tagarro García A, et al. Neumonía adquirida en la comunidad: tratamiento de los casos complicados y en situaciones especiales. Documento de consenso de la Sociedad Española de Infectología Pediátrica (SEIP) y Sociedad Española de Neumología Pediátrica. An Pediatr. 2015;83:217.e1-217.e11.
- Pereda MA, Chavez MA, Hooper-Miele CC, et al. Lung ultrasound for the diagnosis of pneumonia in children: a meta-analysis. Pediatrics. 2015;135:714-22. 8. Úbeda Sansano I, Croche Santander B, Hernández Merino A. Neumonía (v.3/2020). Guía-ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico [en línea] [actualizado el 25/04/2020; consultado el dd/mm/aaaa]. Disponible en http://www.guia-abe.es
- Pernica JM, Harman S, Kam AJ, Carciumaru R, Vanniyasingam T, Crawford T, Dalgleish D, Khan S, Slinger RS, Fulford M, Main C, Smieja M, Thabane L, Loeb M. Short-Course Antimicrobial Therapy for Pediatric Community-Acquired Pneumonia: The SAFER Randomized Clinical Trial. JAMA Pediatr. 2021 Mar 8:e206735.