Pérez-Torres Lobato, María
Pérez Hurtado, José María
Molinos Quintana, Águeda
DEFINICIÓN
Fiebre: Un episodio aislado de temperatura ≥ 38ºC o dos determinaciones superiores a 37.6ºC con menos de seis horas de intervalo entre ellas y sin que puedan ser achacables a la administración de hemoderivados y/o quimioterapia.
Neutropenia: < 500 neutrófilos/mm3 ó < 1000 neutrófilos/mm3 + predecible rápido descenso en las siguientes 24-48 h o tratamiento quimioterápico en los 14 días anteriores.
EVALUACIÓN DIAGNÓSTICA
| HISTORIA CLÍNICA | PX COMPLEMENTARIAS | GRUPO DE RIESGO |
| ANAMNESIS
– Tª y h/días fiebre – Ambiente epidémico – Tipo neoplasia – Receptor TPH (alog. vs autól.) – Último día de QT – Tto corticoides (>2mg/kg >15 días ó >1mg/kg > 30 días) – Uso G-CSF – Profilaxis infecciosa – Cultivos previos (AP infección por SARM o germen MR) – Comorbilidades – Síntomas: DOLOR, diarrea, escalofríos con ascenso Tª, síntomas respiratorios… EXPLORACIÓN 1. Descartar signos de sepsis: TEP,Glasgow,TA,FC,FR,Sat02 2. Descartar focalidad: Exploración minuciosa incluyendo cavidad oral, senos, region perianal, piel, catéter… |
LABORATORIO
Hemograma, bioquímica, PCR, PCT, EAB (si gravedad) MICROBIOLOGÍA – Hemocultivo: de todas las luces catéter, previo inicio antibioterapia. Valorar HC diferencial si sospecha IAC. – Urocultivo: ≤36 meses, focalidad. – Cultivo de todo foco sospechoso infección. – Virus respiratorios si síntomas/ temporada epidémica. – Toxina C. difficile, Virus en heces y coprocultivo si diarrea. – Galactomanano: neo hematológica/neo sólida e infiltrado nodular y/o cavitado o falta de respuesta al tratamiento – PCR de CMV sangre: TPH alogénico primeros 100 días. Añadir PCR VEB y adenovirus en sangre si TPH alto riesgo (cordón, hermanos no haplo-idénticos, donante no emparentado) RADIOLOGÍA Si focalidad. Ver FN con foco |
ALTO RIESGO (AR)
Cualquiera de: 1. TEP alterado, signos sepsis. 2. Neoplasia de alto riesgo1 3. Receptor TPH alogénico 4. TPH autólogo 30 días posteriores al alta TAMO 5. Tto corticoides (>2mg/kg >15 días ó >1mg/kg > 30 días) 6. FR bacteriemia: Tª≥39ºC, fiebre y escalofríos, PCR>70 mg/l 7. Focalidad: dolor abdominal/vómitos persistentes, mucositis severa u otra focalidad distinta a CVA/virasis 8. Neutropenia >7 días 9. <100 neutrófilos/mm3 en neo hematológica o asociado a criterios AR 10. Comorbilidad2 BAJO RIESGO – Ausencia de criterios AR – < 100 neutrófilos en tumor sólido + ausencia criterios AR – >100 neutrófilos en neo hematológica + ausencia criterios AR |
TEP: triángulo de evaluación pediátrica. TPH: trasplante progenitores hematopoyético. QT: quimioterapia. G-CSF: factor estimulante de colonias granulocíticas. SARM: Staph aureus meticilín-resistente. MR: multirresistente. IAC: infección asociada a catéter. CVA: catarro de vías altas.
Neoplasia de alto riesgo:1 Leucemia mieloblástica aguda, linfoma de Burkitt, linfoma/leucemia linfoblástica aguda, neoplasia con diseminación progresiva/enfermedad en recaída que incluya infiltración médula ósea.
Comorbilidades2 insuficiencia hepática/renal, cardiopatía, neumopatía, enfermedad neurodegenerativa…
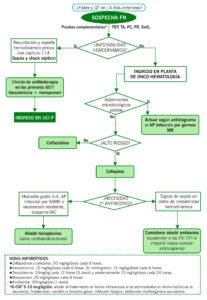
MANEJO DE LA FIEBRE NEUTROPÉNICA SIN FOCO
MANEJO DE LA FIEBRE NEUTROPÉNICA CON FOCO
| NEUMONÍA | |
| Definición | – Fiebre y/o síntomas respiratorios (tos, disnea, expectoración purulenta o cambio o aumento en las secreciones) + infiltrado pulmonar de nueva aparición o progresivo que no puede explicarse por otra patología no infecciosa. |
| Laboratorio/Microbiología | – Urgentes (previo inicio antibioterapia salvo shock séptico): Hemograma, bioquímica, PCR, PCT, hemocultivos, EAB si distrés, tinciones de esputo y cultivo para bacterias, hongos y micobacterias, antígeno de neumococo (> 2 años) y Legionella pneumophila en orina.
– Galactomanano: pacientes con hemopatías malignas, pacientes con neoplasia sólida e infiltrado nodular y/o cavitado o falta de respuesta al tratamiento. – Aspirado nasofaríngeo para test rápido de virus influenza A y B y VRS en temporada invernal. Si resultado negativo y alta sospecha: realizar PCR. – Si disponible, reemplazar test de virus por PCR múltiple. Valorar Film-array (incluye adenovirus) en receptores de alo-TPH primeros 6 meses. – PCR de CMV sangre: si neumonitis/receptores alo-Trasplante primeros 6 meses. |
| Radiología | – Rx de tórax PA si síntomas respiratorios/sospecha de derrame pleural
– TAC de tórax: si Rx tórax normal y clínica respiratoria/si sospecha de aspergilosis o de etiología no infecciosa (metástasis, TEP, progresión enfermedad…). |
| Tratamiento empírico (valorar siempre aislamientos microbiológicos previos) | – NEUMONÍA FOCAL: Cefepima 50 mg/kg c/8h iv
– NEUMONÍA BILATERAL: Cefepima 50 mg/kg/8 h iv +/- ciprofloxacino iv 10-15mg/Kg/d (2 dosis). Si sospecha de germen multirresistente, sustituir por meropenem 50 mg/kg/8 h iv. Añadir: a) Cotrimoxazol 5/25 (TMP/SMX) mg/kg/6 h iv si no profilaxis para P. jirovecii. b) AmB-L (3 mg/kg/día) si paciente de alto riesgo o sospecha/riesgo infección fúngica u hongo filamentoso. c) Azitromicina 10 mg/kg/día si sospecha de neumonía atípica. – PRESENTACIÓN GRAVE: a) Bajo riesgo: Cefepima +/- ciprofloxacino +/- AmB-L b) Alto riesgo: Meropenem + Vancomicina (10 mg/kg/6 h iv) + AmB-L
Para ver tratamiento dirigido, consultar guía PRIOAM: https://guiaprioam.com/indice/infecciones-respiratorias-en-el-paciente-con-neoplasia-maligna/ |
| INFECCIONES DEL APARATO DIGESTIVO | |
| Definiciones | MUCOSITIS: inflamación de la superficie mucosa que recubre el interior del tracto digestivo. Según el grado (OMS): 1(leve)=eritema y dolor; 2(moderada)=úlceras, puede comer sólidos; 3(grave)=requiere dieta líquida; 4(severa)=imposible alimentación oral
ENTEROCOLITIS NEUTROPÉNICA: colitis necrotizante con inflamación del ciego y, frecuentemente, de los tejidos adyacentes. Los síntomas son los de abdomen agudo e incluyen la triada de fiebre, dolor abdominal (de predominio en FID) +/- diarrea acuosa o sanguinolenta. Puede producir vómitos y acompañarse de síntomas de sepsis. ENTERITIS AGUDA: cuadro consistente en disminución de la consistencia/aumento en la frecuencia (>3/día) de las deposiciones acompañado o no de fiebre, dolor abdominal, vómitos. C. difficile es uno de los patógenos más frecuentemente implicados, en relación con hospitalización prolongada y uso de antibióticos de amplio espectro. ENFERMEDAD PERIANAL: se trata de una de las complicaciones potencialmente más graves del paciente neutropénico. Normalmente se acompañan de dolor espontáneo/a la palpación, tumefacción, eritema, lesión hemorroidal/ulceración… |
| Pruebas Complementarias | Laboratorio: Hemograma, bioquímica (incluir perfil hepático), PCR, PCT, hemocultivo.
Si diarrea: coprocultivo, virus en heces (adenovirus, norovirus, rotavirus), toxina C. difficile. Si alo-TPH primeros 6 meses, añadir PCR CMV en sangre y valorar cultivo de parásitos (x3 muestras). Si alteración perfil hepático en alo-TPH primeros 6 meses: PCR CMV, VEB, HHV-6, adenovirus, VVZ/VHS, virus hepatotropos. Ecografía abdominal: focalidad abdominal, signos de abdomen agudo, megalias y/o hipertransaminasemia/patrón de colestasis. TAC abdominal: focalidad abdominal/signos de abdomen agudo con ecografía normal/no concluyente. |
| Tratamiento | 1. MUCOSITIS GRADO 3-4 (CON FIEBRE): cefepima+ teicoplanina. Valorar asociar fluconazol/ aciclovir si sospecha sobreinfección por cándida o herpes.
2. INFECCIÓN ABDOMINAL EN PACIENTE DE BAJO RIESGO: piperazilina-tazobactam 80 mg/kg/dosis cada 6h. Alternativa: cefepima + metronidazol. Si paciente de alto riesgo: añadir amikacina. 3. INFECCIÓN ABDOMINAL CON SIGNOS DE GRAVEDAD: meropenem + amikacina. Valorar añadir Anfotericina B si sospecha de Candidiasis hepato-esplénica. 4. INFECCIÓN POR CLOSTRIDIUM DIFFICILE: – Brote no grave en primoinfección/1ª recaída: metronidazol oral 25-30 mg/kg/día c/6h 10-14 días (máx 500 mg/dosis) – Brote grave1, intolerancia o falta de respuesta a metronidazol en primoinfección o 1ª recaída: vancomicina oral 30-40 mg/kg/día c/6h (máx 125 mg/dosis) 10-14 días o enemas de vancomina +/- metronidazol iv (7,5 mg/kg/dosis c/8h). – 2ª recaída: Vancomicina 125 mg/6 h vo x10-14 días, seguido de Vancomicina vo dosis decrecientes: 125 mg/12h x7días, 125 mg/24 h x7 días, 125 mg/48 h x8 días (4 dosis), 125 mg/72 h x15 dias (5 dosis). *En brotes graves/2ª recaídas valorar tto combinado o añadir Ig (400 mg/kg semana x 2-3 dosis) 5. INFECCIÓN PERIANAL/RECTAL: piperacilina-tazobactam +/- amikacina. – Si datos de gravedad/paciente de alto riesgo: meropenem + amikacina. – Si sospecha de infección estreptocócica asociar clindamicina 25-40 mg/kg/día c/6-8 h en 30 min (máx 2,7 g/día). IMPORTANTE: manejo sintomático (hidratación, control del dolor, nutrición parenteral + dieta absoluta, necesidad SNG), interconsulta a cirugía. |
Brote grave:1 Cualquiera de: 1) Síntomas y signos clínicos y analíticos de colitis severa por C. difficile; 2) Requerimiento de ingreso en UCI-P; 3) Presencia de al menos 2 de los siguientes factores: Leucocitosis>15.000, neutrófilos segmentados > 20% del recuento de leucocitos, aumento de la creatinina ≥1,5 veces el valor basal, lactato sérico > 2,5 mmol/l, Tª > 38.5 ◦C, >10 deposiciones diarreicas diarias, presencia de íleo paralítico o signos de peritonitis, albúmina < 2,5 mg/dl, evidencia de colitis en px de imagen.
BIBLIOGRAFÍA
- Lehrnbecher T, Robinson P, Fisher B, Alexander S, Ammann RA, Beauchemin M, et al. Guideline for the management of fever and neutropenia in children with cancer and hematopoietic stem-cell transplantation recipients: 2017 update. J Clin Oncol. 2017;35(18):2082–94.
- Davis K, Wilson S. Febrile neutropenia in paediatric oncology. Paediatr Child Health (Oxford). 2020 Mar;30(3):93-97.
- Haeusler GM, Phillips R, Slavin MA, Babl FE, De Abreu Lourenco R, Mechinaud F, et al. Re-evaluating and recalibrating predictors of bacterial infection in children with cancer and febrile neutropenia. EClinicalMedicine [Internet].2020;23:100394.
- Alison G. Freifeld, Eric J. Et al. Clinical Practice Guideline for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer: 2010 Update by the Infectious Diseases Society of America Clinical Infectious Diseases 2011;22:56–93.
- Paul M, Dickstein Y, Schlesinger A, Grozinsky-Glasberg S, Soares-Weiser K, Leibovici L. Beta-lactam versus beta-lactam-aminoglycoside combination therapy in cancer patients with neutropenia. Cochrane Database Syst Rev. 2013 Jun 29;2013(6).
- McMullan BJ, Haeusler GM, Hall L, Cooley L, Stewardson AJ, Blyth CC, et al. Aminoglycoside use in paediatric febrile neutropenia – Outcomes from a nationwide prospective cohort study. PLoS One. 2020;15(9):1–12.
- G.Maschmeyer, T.Beinert, D.Buchheidef et al. Diagnosis and antimicrobial therapy of lung infiltrates in febrile neutropenic patients: Guidelines of the infectious disease working party of the German Society of Haematology and Oncology. European Journal of cancer. Eur J Cancer. 2009; 45:2462-72.
- Alvarez AM, Rathore MH. Clostridium difficile Infection in Children. Advances in Pediatrics. 2019; 66;263–80).
- Castagnola E, Ruberto E, Guarino A. Gastrointestinal and liver infections in children undergoing antineoplastic chemotherapy in the years 2000. World J Gastroenterol. 2016;22(25):5853–66.
- Saullo JL,Polage CR. Tackling Infectious Diarrhea in Hematopoietic Cell Transplantation. Clin InfectDis. 2020;71 (7):1701–03.